سولفات چیست؟ و انواع آن
در علم شیمی معدنی به مجموعه ای از ترکیبات یونی از سولفور (گوگرد)، سولفات گفته می شود. نام سولفات (Sulfate) برگرفته شده از ریشه لغوی بریتانیایی آن می باشد. جرم مولی این ترکیبات شیمیایی معدنی به مقدار 96.07 گرم بر مول می باشد. از این ترکیبات در صنایع مختلف به صورت نمک ها، مشتقات اسیدی و پراکسید های سولفات، استفاده می شود.
کاتالوگ معرفی مواد شیمیایی فامکو
مشخصات شیمیایی سولفات ها
سولفات ها در واقع نمک های اسید سولفوریک (H2SO4) بوده و از این مواد تشکیل می شوند. استر های سولفات آلی، همچون دی متیل سولفات، ترکیباتی با پیوند کووالانسی هستند که در واقع استر های سولفوریک اسید می باشند. توجه داشته باشید که بیشتر سولفات ها، سولفات های محلول در آب هستند، اما به طور استثنا مشتقاتی از جمله سولفات استرانسیم، سولفات باریم، سولفات کلسیم و سولفات سرب (ll) حلالیت کمتری در آب داشته و از سولفات های نامحلول به شمار می روند. شایان ذکر است سولفات رادیوم به عنوان نامحلول ترین سولفات شناخته می شود. یون سولفات می تواند به عنوان یک لیگاند عمل کند که توسط یک اکسیژن (تک دندانه) یا توسط دو اکسیژن به عنوان یک کلات یا یک پل متصل می شود.
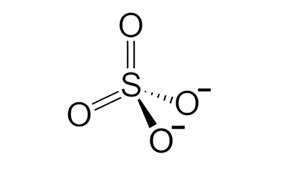
ساختار شیمیایی و عدد اکسایش سولفات ها
سولفات ها با فرمول پایه -SO42 ترکیباتی آنیونی هستند که از یک اتم گوگرد مرکزی و 4 اتم اکسیژن به صورت آرایش چهار وجهی تشکیل شده اند. طبق تئوری اکتت یا هشت تایی در علم شیمی، اتم گوگرد دارای عدد اکسایش 6+ و اتم های اکسیژن هر کدام 2- هستند. بدین ترتیب بار کلی یون سولفات، 2- می باشد. لازم به ذکر است باز مزدوج این ترکیبات، یون بی سولفات یا هیدروژن سولفات (-HSO4) می باشد که مایعی خورنده، متراکم، بی رنگ و روغنی است. ترکیب بی سولفات، خود نیز باز مزدوج اسید سولفوریک است.
آنالیز تشخیصی آنیون سولفات
به منظور آنالیز وزنی سولفات از مشتق باریم استفاده می کنند. به این ترتیب که در طی اضافه کردن محلولی حاوی اکثر نمک های باریم (برای مثال کلرید باریم) به محلول حاوی یون های سولفات، رسوب سفید رنگی تشکیل می شود که سولفات باریم می باشد. این آزمایش جهت تشخیص وجود آنیون سولفات انجام می شود.
انواع سولفات و کاربرد آن ها
سولفات ها در انواع مختلف دارای کاربرد های گسترده ای می باشند که در زیر به بعضی از انواع ترکیبات آن اشاره شده است.
- سولفات کلسیم: گچ، فرم طبیعی ماده معدنی سولفات کلسیم هیدراته می باشد که از آن برای تولید پلاستر استفاده می شود. سالانه حدودا 100 میلیون تن از این ترکیب در صنعت ساختمان سازی استفاده می شود.
- سولفات مس یا ویتریول آبی: یک قارچ کش بوده و در صنعت آبکاری به عنوان یک الکترولیت کاربرد دارد.
- سولفات آلومینیوم: این ترکیب بیشتر به عنوان یک منعقد کننده در صنعت تصفیه آب و فاضلاب کاربرد دارد.
- سولفات آهن: شکل رایج آهن در مکمل های معدنی بوده که به عنوان ویتریول سبز نیز شناخته می شود و در مصارف صنعتی، دارویی و کشاورزی بسیار کاربردی است.
- سولفات منیزیم یا نمک اپسوم: در حمام های درمانی و به عنوان کود کشاورزی کاربرد دارد.
- سولفات روی: ویتریول سفید، به عنوان ماده افزودنی غذایی در صنعت کشاورزی موجب بهبود عملکرد خاک و رشد گیاهان استفاده می شود.
- سولفات سدیم: این ماده یکی از پر مصرف ترین مواد شیمیایی در جهان بوده که در تولید محصولات شوینده، شیشه سازی و همچنین صنعت کاغذ استفاده می شود.
- سولفات منگنز: از این ترکیب معدنی به منظور تامین منگنز مورد نیاز خاک و به عنوان کود کشاورزی یا باغبانی جهت تغذیه گیاهان استفاده می شود.
- SLS و SLES: سدیم لوریل سولفات و سدیم لوریل اتر سولفات که هر دو از ترکیبات رایج و بسیار مهم در شوینده ها و به خصوص شامپو ها هستند.
روش تولید سولفات
این مواد اغلب به طور طبیعی و توسط میکروارگانیسم های بی هوازی، که به باکتری های کاهنده هیدروژن معروفند، تولید می شوند. این باکتری ها اغلب در رسوبات یا دریچه های آتشفشانی، دریا ها و اقیانوس ها زندگی می کنند. این میکروارگانیسم ها منبع غذایی و انرژی خود را از طریق اکسیداسیون ترکیب های آلی با هیدروژن و در نتیجه کاهش سولفات تامین می کنند.
اما روش های تولید ترکیبات سولفاته به روش صنعتی بدین گونه است که اسید سولفوریک را با خود فلزات، هیدروکسید های فلزی یا اکسید های فلزی واکنش می دهند. معادله واکنش بعضی از این سولفات های فلزی در زیر نشان داده شده است. نماد سولفات -SO42 می باشد.
Zn + H2SO4 → ZnSO4 + H2
CdCO3 + H2SO4 → CdSO4 + H2O + CO2
Cu(OH)2 + H2SO4 → CuSO4 + 2H2O
همچنین در روش دیگر با اکسیداسیون سولفید ها یا سولفیت های فلزی تولید می شود.
حمله سولفات ها در بتن
این واکنش به صورت کلی شامل ترکیب شدن آنیون های سولفات با آهک و آلومینات هیدراته در ساختار بتن شده و کلسیم سولفات و کلسیم سولفو آلومینات (اترینگایت) را تشکیل می دهد. حجم این فرآورده ها بیشتر از حجم مواد اولیه موجود در ساختار بتن بوده، در نتیجه موجب تورم و ترک خوردگی بتن سخت می شوند. به این ترتیب بعد از تشخیص علت آسیب دیدگی بتن، به منظور ترمیم و همچنین جهت جلوگیری از حمله سولفاتی، بتن ها را باید با مواد مقاوم از جمله بتن نفوذ ناپذیر (به عنوان مثال سیمان مقاوم به حمله سولفاتی)، مقاوم سازی کرد. سیمان نوع 2 و نوع 5 پرتلند به دلیل درصد کلسیم آلومینیت پایین از جمله این مواد مقاوم به حساب می آید. همچنین از موادی مانند خاکستر بادی، میکروسیلیس و همچنین پوزولان های طبیعی نیز به عنوان جایگزین سیمان می توان استفاده نمود. مقاوم سازی بتن موجب افزایش مقاومت سازه های بتنی و همچنین افزایش طول عمر این سازه ها می شود.
سولفات در مصارف آرایشی و بهداشتی
سه نمونه از مشتقات رایج این ماده در صنعت آرایشی و بهداشتی در زیر نام برده شده است:
- سدیم لوریل سولفات
- سدیم لوریل اتر سولفات یا همان سدیم لورت سولفات
- آمونیوم لوریل سولفات
سولفات در شامپو برای چیست؟
این مواد به عنوان عامل کف کننده در محصولات شوینده و شامپو ها به کار می روند. در ادامه به مزایای شامپو های سولفات دار و ویژگی های آن ها پرداخته شده است.
مزایا شامپو ها سولفات دار
- پاک کننده های قوی جهت تمیز کنندگی کامل چربی کف سر و عدم ایجاد شوره سر هستند.
- از لحاظ اقتصادی مقرون به صرفه و در دسترس هستند.
- با ترکیبات دیگر قابل ملایم سازی می باشند (استفاده از بتائین).
- چه از لحاظ ایمنی و چه از نظر مراجع قانونی این محصولات مورد تایید می باشند.
موارد احتیاط حین مصرف شامپو های سولفات دار
- مهم ترین موضوعی که برای استفاده از محصولات حاوی سولفات می بایست در نظر گرفته شود، تحریک کنندگی آن ها است که اگر طبق شرایط اصولی فرموله شوند و از غلظت بالای این ترکیبات استفاده نشود، می توانند باعث کاهش اثر تحریک کنندگی و بهینه شدن آن ها گردند. نشانه های تحریک کنندگی، خارش، پوسته پوسته شدن، ایجاد زخم، قرمزی و خشکی پوست می باشد.
- به منظور افزایش خاصیت نگهداری محصولات شوینده بهداشتی و شامپو ها، در فرمولاسیون این مواد به همراه سولفات ها از موادی همچون سوربات پتاسیم و ایزوتیازولین استفاده می شود.
آیا سولفات ها مضر هستند؟
باید دید منظورمان از مضر بودن چیست؟ اگر منظور خاصیت تحریک کنندگی این ترکیبات باشد، بله محرک و تحریک کننده بوده، اما سرطانزا نیستند. اگر از ترکیبات خالص و غلیظ سولفات دار بر روی پوست سر خود استفاده کنید، پس از مدتی پوست تحریک شده و شروع به قرمزی می کند. همچنین ورود کف شامپو های سولفات دار به چشم، خارش و سوزش را به همراه دارد. بنابراین هرچه غلظت این ترکیبات در شامپو ها بیشتر باشد، خاصیت تحریک کنندگی هم بیشتر شده و می تواند منجر به خشکی مو ها نیز شود.
آیا ترکیبات سولفات سرطانزا هستند؟
این موضوع بر اساس مقالات علمی معتبر در دنیا مورد بررسی قرار گرفته است. یک مجله معتبر در آمریکا با نام توکسیکولوژی (Toxicology)، که به طور کلی در مورد مسمومیت زایی ترکیبات صحبت می کند، در سال 1983 به صورت اختصاصی در مورد آن ها مقاله نوشته است. طبق تحقیقات، این مجله نتایج مهم زیر را در مورد دو ترکیب رایج سولفات ها که شامل سدیم لوریل سولفات و آمونیوم لوریل سولفات می شود، ارائه داده است:
- سولفات ها سرطانزا نبوده و ترکیباتی ایمن شمرده می شوند.
- سولفات ها در غلظت کمتر از 2 درصد تحریک کننده نیستند.
- هر چه غلظت سولفات های مصرفی در ترکیبات از 2 درصد بیشتر باشد، خاصیت تحریک کنندگی پوست و خشک کنندگی مو ها افزایش می یابد.
راهکار های کاهش تاثیر تحریک کنندگی سولفات ها
به منظور کاهش اثر تحریک کنندگی این شامپو ها از روش ها و ترکیباتی استفاده می شود که در زیر به دو مورد بسیار مهم آن اشاره شده است.
- فرمولاسیون شامپو: ترکیباتی وجود دارند که در کنار سولفات ها، موجب کاهش تحریک کنندگی این دسته از مواد شیمیایی می شوند. یکی از مشهور ترین این ترکیبات، بتائین ها (Betaines) هستند. به این ترتیب به منظور استفاده از سولفات ها در فرمولاسیون شامپو ترکیباتی جهت کاهش تحریک کنندگی، ملایم شدن و بهبود خاصیت اضافه می گردد.
- آبکشی صحیح: هنگام شست و شو مو ها، آبکشی صحیح موجب پاک شدن تمامی ترکیبات شامپو و در واقع ترکیبات سولفات از روی پوست سر شده از این رو احتمال تحریک پوست کاهش خواهد یافت.
چرا استفاده از شامپو های بدون سولفات توصیه می شود؟
حالا که با این ترکیبات شیمیایی و ویژگی های آن در شوینده ها آشنا شدیم، بهتر است به مزایا و معایب شامپو های بدون سولفات بپردازیم که در زیر به برخی از آن ها اشاره شده است.
مزایا شامپو های بدون سولفات
- استفاده از شامپو های بدون سولفات برای موهای کراتینه یا رنگ شده توصیه می شوند چرا که موجب ماندگاری بیشتر و عدم آسیب رساندن به پوست سر یا خشکی مو ها می شوند.
- شامپو های فری سولفات ملایم بوده و موجب تحریک پوست نیز نمی شوند.
نکات مهم در رابطه با شامپو های بدون سولفات
- قدرت پاک کنندگی کم: شامپو های بدون سولفات قدرت تمیز کنندگی کمتری نسبت به شامپو های حاوی سولفات دارند. همچنین در صورتی که چربی های کف سر به خوبی پاک نشوند، موجب انباشت چربی ها و رشد قارچ می شود که در نهایت شوره سر را به همراه دارد.
- ریزش مو: در اثر فشار به پیاز مو هنگام شست و شوی سر، مقاومت ریشه مو کاهش و ریزش آن زیاد خواهد شد.
- قیمت بالا: شامپو های بدون سولفات قیمت بیشتری دارند، همچنین به دلیل کف کمتر و عدم پاک کنندگی مناسب، به مقدار بیشتری مصرف می شوند، در نتیجه موجب افزایش هزینه مصرفی خواهند شد.
روش شناسایی شامپو های فری سولفات
به صورت کلی برای اینکه یک شامپو را جز محصولات بدون سولفات (Sulfate Free) به حساب بیاوریم، هیچ یک از فرم های دیگر آن نیز، برای مثال ترکیبات زیر، در فرمولاسیون آن نمی بایست وجود داشته باشد:
- سدیم لوریل سولفات
- سدیم لوریل سولفواستات
- سولفات منیزیم
- آمونیوم لوریل سولفات
- الفین سولفونات سدیم C14-16
- سولفات آلومینیوم
- اتیل PEG-15 کوکامین سولفات
- آمونیوم لورت سولفات
- سدیم زایلن سولفونات
- دودسیل بنزن سولفونات چای
- آمونیوم لوریل اتر سولفات
- سدیم میرت سولفات
- دی اکتیل سدیم سولفوسوکسینات
- سدیم لوریل سارکوزینات
حضور هر یک از مشتقات این ترکیبات در فرمولاسیون منجر به بروز ویژگی های تحریک کنندگی شامپو خواهد بود و به این ترتیب باید ملایم سازی انجام گیرد.
- سدیم لورت سولفات
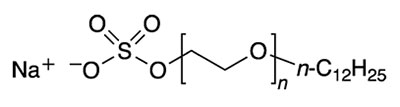
- آمونیوم لوریل سولفات
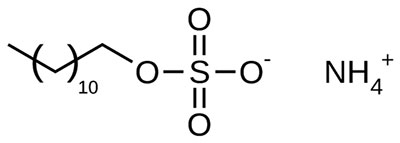
تاثیرات محیطی سولفات ها
این ترکیبات شیمیایی به صورت ذرات میکروسکوپی (آئروسل ها) ناشی از سوخت فسیلی و احتراق زیست توده به وجود می آیند. این ترکیبات موجب افزایش اسیدیته جو شده و باران اسیدی را تشکیل می دهند. باکتری های بی هوازی کاهنده سولفات همچون Desulfovibrio desulfuricans و D.vulgaris می توانند پوسته سولفات سیاه را که اغلب ساختمان ها را کدر می کند، حذف کنند.
تاریخچه سولفات ها
اولین بار توصیف پیوند به مفهوم مدرن توسط دانشمندی با نام گیلبرت لوئیس و بر مبنای قانون هشتایی قرار گیری الکترون ها در اطراف اتم ها بود.
حدودا از سال 1800 استفاده از ترکیبات سولفات دار به شکل های مختلف رواج داشته است. اما در سال 1930 برای اولین بار استفاده از این ترکیبات به صورت گسترده و تجاری توسط شرکت پراکتر اند گمبل (Procter & Gamble) جهت تولید شامپو مورد استفاده قرار گرفت که امروزه در یکی از موزه های آمریکا به عنوان افتخارات این شرکت نگهداری می شود.












دیـــدگاهها
شما هم درباره این کالا دیدگاه ثبت کنید.
امتیاز: