فروش اسید سولفوریک
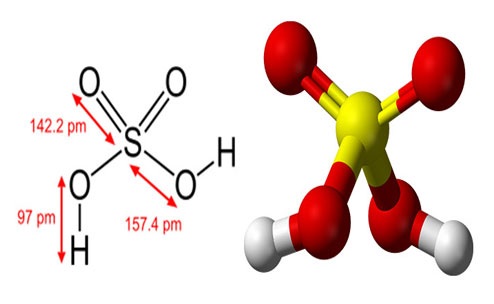
این ماده به صورت طبیعی در گازهای خارج شده از آتشفشان وجود دارد. ساختار سولفوریک اسید شامل یک اتم گوگرد، چهار اتم اکسیژن و دو اتم هیدروژن می باشد. شاید این سوال برای شما پیش آمده باشد که اسید سولفوریک چه رنگی است؟ باید بدانید که اسید سولفوریک مایعی شفاف و بی رنگ می باشد.

انواع اسید سولفوریک بر اساس خلوص
اسید سولفوریک در گریدهای زیر تولید می شود:
- اسید سولفوریک صنعتی: اسید سولفوریک صنعتی به عنوان یکی از قوی ترین اسیدهای موجود در بازار، بیشترین مصرف را در صنایع مختلف و به منظور تولید محصولات گوناگون و کاربری های متفاوت از جمله مواد شوینده، پالایش نفت، تولید اسید باتری و غیره دارد.
- اسید سولفوریک آزمایشگاهی: این گرید از سولفوریک اسید در بسیاری از آزمایش های شیمی همچون آماده سازی نمونه جهت تعیین درصد آب اکسیژنه در محصولات مختلف قابل استفاده است. اسید سولفوریک آزمایشگاهی همچنین به دلیل قدرت بالای آن، برای شست و شوی ظروف آزمایشگاهی که حاوی رسوب هستند استفاده می شود.
- اسید سولفوریک خوراکی: در برخی از نقاط مانند اروپا (طبق استاندارد E513 اتحادیه اروپا) تولید کننده های مواد غذایی از محلول های بسیار رقیق اسید سولفوریک خوراکی برای استفاده در مواد غذایی به عنوان کنترل کننده pH و نگهدارنده به منظور جلوگیری از رشد باکتری و میکروب های مضر استفاده می کنند. اسید سولفوریک خوراکی مصارف بسیار خاصی داشته و در حال حاضر موجود نمی باشد.
این اسید همچنین در 3 خلوص مختلف شامل موارد زیر تولید می شود که هر کدام قیمت های متفاوتی نیز دارند:
- سولفوریک اسید 98 درصد
- سولفوریک اسید 50 درصد
- سولفوریک اسید 35 درصد
اسید سولفوریک 98 درصد یعنی چه؟
اسید سولفوریک 98 درصد غلیظ بوده و از خلوص بالایی برخوردار است و پایداری بیشتری دارد. همچنین خورندگی بالایی برای فلزات، بافت زنده و غیره دارد.
مشخصات سولفوریک اسید
اکنون با مشخصات و خواص سولفوریک اسید آشنا خواهیم شد.
مشخصات اسید سولفوریک
| فرمول شیمیایی |
H2SO4 |
| جرم مولی |
98.078 گرم بر مول |
| شکل ظاهری |
مایع بی رنگ و شفاف، بدون بو |
| دانسیته |
1.84 گرم بر سانتی متر مکعب |
| نقطه ذوب |
10 درجه سانتی گراد |
| نقطه جوش |
337 درجه سانتی گراد |
| حلالیت در آب |
کاملا محلول، واکنش گرماده |
| گرانروی (در دمای 20 درجه سانتی گراد) |
26.7 سانتی پواز |
شکل ظاهری اسید سولفوریک چگونه است؟
این ماده بسته به میزان خالص بودن آن در طبیعت از نظر ظاهری متغیر می باشد و در واقع بی رنگ تا قهوه ای تیره رنگ، روغنی، متراکم، بی بو و خورنده است، اما به صورت کلی اسید سولفوریک مایعی بی رنگ در نظر گرفته می شود.
مشخصات شیمیایی اسید سولفوریک
اسید سولفوریک 98 درصد خورنده است و بخش عمده ای از باران اسیدی را تشکیل می دهد. قطرات آب به هنگام بارش با آلاینده های معلق در هوا، واکنش می دهند و تولید اسید می کنند. در واقع قطرات آب با فلزات واکنش می دهد و هر چه دما بالاتر رود میزان این واکنش بیشتر خواهد شد اما تاثیری روی جیوه و سرب ندارد. سولفوریک در لیست مواد خطرناک قرار گرفته است. اسید سولفوریک به دلیل تمایل زیاد برای جذب بخار آب، به طور طبیعی و کاملا خالص روی زمین وجود ندارد.
واکنش اسید سولفوریک با فلزات چگونه است؟ واکنش اسید سولفوریک با اجسامی که در آن ها فلز وجود دارد و بصورت کلی با فلزات سریعا واکنش می دهد و مثل تمامی عناصر شیمیایی هرچه دما بیشتر باشد میزان و سرعت واکنش نیز افزایش پیدا می کند. واکنش شیمیایی اسید سولفوریک با اجسام فلزی دارای یک استثناء می باشد، چون که این اسید بسیار قوی بر روی فلزات جیوه و سرب هیچ اثری ندارد.
سولفوریک اسید مایعی با نقطه جوش بالا، در حدود 10 درجه سانتی گراد می باشد، همچنین ویسکوز است و گرانروی زیادی دارد. این ماده دارای مولکول هایی با گشتاور قطبی است که می توانند با یکدیگر پیوند هیدروژنی برقرار کنند، همین شرایط مولکولی سبب می شوند که سولفوریک اسید به خوبی در آب حل شود، بنابراین می تواند محلول های اسیدی بسیار مختلفی تولید کند. سولفوریک اسید یک مایع بسیار قطبی است و دارای یک قطر دی الکتریک در حدود 100 می باشد.
فرآیند تفکیک اسید سولفوریک
این ماده از هدایت الکتریکی بالایی برخوردار است، به گونه ای که طی فرآیندی به نام اتوپروتولیز در اثر تفکیک از طریق پروتون سازی (+H) و توانایی جذب این هیدروژن اسیدی به وسیله جفت الکترون غیر پیوندی ایجاد می شود. اسید سولفوریک رایج ترین ماده شیمیایی برای کاهش pH در تصفیه آب است، اگرچه در بعضی مواقع از دی اکسید کربن نیز به خصوص در رابطه با آهک برای افزایش قلیاییت استفاده می شود.
لازم به ذکر است تفکیک اسید سولفوریک طی دو مرحله و ابتدا به صورت کامل (به دلیل پایداری فرم رزونانسی در این مرحله) تفکیک می شود:
H2SO4 + H2O → HSO4- + H3O+
در مرحله دوم به دلیل سخت جدا شدن یون +H3O از آنیون هیدروژن سولفات، تفکیک به صورت کامل نبوده و در نهایت واکنش تعادلی خواهد بود:
HSO4- + H2O ⇔ H3O+ + SO42-
تولید اسید سولفوریک
جابر بن حیان، کاشف سولفوریک اسید، این ماده را از طریق تقطیر خشک کانی هایی که شامل سولفات آهن (زاج سبز) و سولفات مس (کات کبود) بودند به دست آورد. بعدها افراد دیگری مانند جان گلوبر ، جان روبک و جوزف گیلوساک روش های دیگری را برای تولید این ماده ارائه دادند. امروزه اسید سولفوریک در صنعت و تولید مواد شیمیایی مختلف کاربرد دارد، بنابراین نیاز به روشی برای تولید بالا و مقرون به صرفه این ماده است. از واکنش SO3 با آب می توان اسید سولفوریک تولید کرد اما این روش به دلیل گرمازا بودن واکنش و وجود مشکلات در کنترل واکنش عملی نیست از این رو برای تولید این ماده از روش تماسی در مجاورت کاتالیزور استفاده می شود.
اسید سولفوریک با روش های دیگری نظیر فرآیند محفظه سرب و فرآیند اسید سولفوریک مرطوب و همچنین با استفاده از منابع مهم دی اکسید گوگرد حاصل از استخراج و تصفیه فلزات و سنگ های فلزی همچون سولفید ها نیز تهیه می شود. به عنوان مثال کشور چین یکی از تولید کننده های گوگرد با استفاده از سنگ پیریت (سنگ معدن سولفید آهن) می باشد.

مراحل تولید سولفوریک اسید با استفاده از فرایند مجاورت گوگرد
در مرحله نخست گوگرد در مجاورت اکسیژن، اکسید شده و گوگرد دی اکسید به دست می آید. گوگرد مذاب در کوره پاشیده می شود و در انفجار هوای خشک در حدود 1300 کیلوگرم سوزانده می شود:
S + O2 → SO2
سپس گوگرد دیاکسید در مجاورت یک کاتالیزگر و در واکنش با اکسیژن اضافی به SO3 یا گوگرد تری اکسید، اکسید میشود:
SO2 + O2 → SO3
درنهایت از واکنش گوگرد تریاکسید با آب، محلول سولفوریک اسید تولید میشود. در ساخت یک تن اسید سولفوریک، یک تن بخار با فشار بالا نیز تولید می شود:
SO3 + H2O → H2SO4
این واکنش در دمای معمولی سرعت پایینی دارد به همین منظور واکنش را در محیطی با دمای ۴۰۰ تا ۷۰۰ درجه سانتی گراد انجام می دهند و برای واکنش از کاتالیزور وانادیم پنتوکسید (V2O5) استفاده می شود.
حال SO3 را به اسید سولفوریک غلیظ وارد می کنند که از این واکنش پیرو سولفوریک اسید بدست می آید:
H2SO4(l)+SO3(g) → H2S2O7(l)
اگر به پیرو سولفوریک اسید مقدار مشخصی آب اضافه گردد اسید با غلظت مورد نظر حاصل می شود:
H2S2O7(l)+H2O(l) → 2H2SO4(l)
روش آزمایشگاهی سنتز اسید سولفوریک
تولید اسید سولفوریک با استفاده از روش های آزمایشگاهی مختلف که شامل موارد زیر است، نیز انجام می گیرد:
- از واکنش گاز گوگرد دی اکسید با هیدروژن پراکسید (آب اکسیژنه):
SO2 + H2O2 → H2SO4
- با استفاده از الکترولیز محلول مس (ll) سولفات که در این فرآیند، کاتد باید یک فلز با رسانایی خوب و آند از جنس پلاتین یا زغال (به منظور عدم واکنش با محلول) باشد.
رقیق سازی محلول اسید سولفوریک
سولفوریک اسید بسیار سنگین است و در غلظت های بالا بسیار خورنده بوده و خشک کننده قوی است. اسید سولفوریک رقیق با هر نسبتی در آب حل می شود ولی در حالت غلیظ، ریختن آب بر روی آن، بسیار خطرناک است و باعث پاشش اسید به اطراف و حتی انفجار می شود. پس ممکن است با توجه به کاربرد، به رقیق کردن این اسید نیاز باشد.
به منظور رقیق کردن اسید سولفوریک غلیظ و تهیه اسید با غلظت دلخواه، ابتدا مقدار اسید سولفوریک و آب مقطر را محاسبه کرده، سپس به منظور به حجم رساندن از ظروف آزمایشگاهی همچون بالن استفاده می کنیم. به این صورت که ابتدا بالن را از مقداری آب مقطر پر کرده و روی استیرر می گذاریم تا حین اضافه کردن اسید سولفوریک به بالن، محلول یکنواخت شده و از تجمع اسید در انتهای ظرف و داغ کردن آن جلوگیری کند.
همچنین ذکر این نکته ضروری است که باید مدتی صبر کرد تا بالن خنک شود، زیرا در صورت به حجم رساندن در این مرحله به دلیل دمای بالای محلول و تبخیر شدن، محلول سازی به درستی انجام نمی گیرد و غلظت اشتباه خواهد شد. در انتها نیز بالن را با آب مقطر تا خط نشانه به حجم می رسانیم.
این نکته بسیار مهم است که اسید سولفوریک را به آب مقطر اضافه کنیم، زیرا این واکنش بسیار گرماده بوده و در صورت رعایت نکردن نکات ایمنی همچون پوشیدن دستکش و استفاده از عینک، ممکن است اسید به اطراف پاشیده شود و منجر به صدمات جبران ناپذیری شود. همچنین به سبب عدم آسیب رسانی بخار های این اسید قوی بهتر است این آزمایش زیر هود آزمایشگاهی انجام شود.
بازار جهانی اسید سولفوریک
اسید سولفوریک به عنوان یک اسید معدنی و از قوی ترین اسید ها در کنار هیدروکلریک اسید و نیتریک اسید به شمار می رود، به گونه ای که لقب سلطان اسید ها را به خود داده است. از گذشته مصرف این اسید در صنایع مختلف در سراسر جهان رواج داشته و تا به امروز نیز تولید و مصرف آن به تبع تقاضای زیاد روند صعودی داشته است. مصرف اسید سولفوریک در صنایع، به طور گسترده و مهم می باشد تا جایی که تولید این اسید، بیانگر قدرت صنعتی یک کشور است.
کاربرد اسید سولفوریک
اسید سولفوریک یکی از مواد پرکاربرد در صنایع مختلف می باشد که در ادامه شرح داده می شود:
- کاربرد اسید سولفوریک در تولید مواد شوینده:
اسید سولفوریک قدرت هیدرولیز بسیار قوی دارد و قادر به حل نمودن چربی ها و لیپیدها می باشد. لذا به عنوان حلال چربی ها و لیپیدها در تولید شوینده ها مورد استفاده قرار می گیرد.

- کاربرد سولفوریک اسید در تولید کودهای شیمیایی:
اسید سولفوریک کشاورزی یکی از پرکاربردترین مواد شیمیایی در جهان است. این اسید بیشترین استفاده را در تولید کودهای شیمیایی و جبران کمبود گوگرد خاک دارد. اسید سولفوریک کشاورزی میزان قلیایی بودن خاک و آب را کاهش می دهد تا تهویه خاک به درستی انجام شود. حدود 60 درصد از بازار مصرف این ماده، مختص به تولید این کودها می باشد.

از اسید سولفوریک جهت تولید کود آمونیوم سولفات استفاده می شود، این کود برای جبران گوگرد در خاک، مناسب است. زمانی که اسید سولفوریک را به خاک اضافه می کنیم، با آهک های موجود در خاک واکنش می دهد و باعث تولید سولفات کلسیم آبدار می شود که به عنوان گچ کشاورزی معروف است. این واکنش همچنین باعث تولید سولفات منیزیم می شود. از سولفوریک اسید جهت تولید کود هایی همچون سوپر فسفات ها و فسفات آمونیوم نیز استفاده می شود.
از مزایای اسید سولفوریک 98 درصد برای باغ های کشاورزی، مزارع و باغچه ها این است که میزان قلیایی بودن خاک و آب را کاهش می دهد. چنانچه از این ماده به صورت منظم برای خاک استفاده شود، باعث می شود که تهویه خاک به درستی انجام شود و میزان نفوذ پذیری خاک افزایش یابد. در صورت استفاده از اسید سولفوریک میزان شوری خاک کاهش پیدا می کند.
یکی دیگر از موارد استفاده اسید سولفوریک کشاورزی، استفاده از آن برای نفوذ پذیری آب و هوا در خاک رس است، نفوذ پذیری هوا و آب در خاک رس به کندی صورت می گیرد. گاها بعد از چندین روز آبیاری هم، آب به خاک رس نفوذ نمی کند. همین موضوع باعث می شود تهویه خاک به درستی انجام نگیرد و ریشه گیاه آسیب ببیند. اسید سولفوریک این مشکل را حل می کند.
ریشه درختان پسته به تهویه بسیار حساس می باشد و کشاورزان زیادی به دلیل عدم مرغوبیت خاک ضررهای زیادی دیده اند. اسید سولفوریک به عنوان یک ماده و کود شیمیایی قوی عمل می کند و باعث می شود که مشکلات کشاورزان در زمان استفاده از این گونه خاک ها حل شود.
اما در استفاده از اسید سولفوریک به عنوان کود باید این موضوع در نظر گرفته شود که کود دادن زیاد به زمین های زراعی باعث می شود که حاصلخیزی خود را از دست بدهند، لذا در استفاده از آن باید احتیاط شود، مثلا زمانی که سیب زمینی غده بسته است، به هیچ عنوان نباید به آن کود داد. همچنین از غلظت های کم سولفوریک اسید برای خشک کردن میوه ها و جذب آب درون آن استفاده می شود.
- کاربرد اسید سولفوریک در پالایش نفت:
ترکیبات نفتی محیط زیست را به شدت آلوده می کنند و سبب خوردگی در دستگاه ها و تجهیزات پالایشگاه می شوند. در پالایش نفت دو نوع تصفیه شیمیایی و تصفیه با هیدروژن داریم که پالایش با اسید سولفوریک از نوع تصفیه شیمیایی است.

اسید سولفوریک، ماده شیمیایی است که برای تبدیل ترکیبات اتیلنی به استرهای محلول در اسید، استفاده می شود و برای تصفیه فرآوردههای سفید مثل بنزین ها و نفت سفید، مورد استفاده قرار می گیرد. هدف آن خنثی نمودن ترکیبات بازی، حذف ترکیبات اکسیژن دار و اکسید کرده مرکاپتانها به دیسولفیدهای کم ضررتر است.
- کاربرد اسید سولفوریک در اسید باتری:
منظور از اسید باتری، اسیدی است که در انواع باتری ها از جمله باتری خودروها استفاده می شود. مایع داخل باطری از مخلوط اسید سولفوریک و آب مقطر به دست می آید. در واقع اسید باتری رقیق شده اسید سولفوریک می باشد چون اسید را نمی توان به راحتی رقیق نمود و باید از دستگاه رقیق کننده قوی استفاده کرد. باتری دستگاهی است که انرژی الکتریکی را در حالت شیمیایی در خود ذخیره می کند تا در زمان نیاز مورد استفاده قرار بگیرد. اساس کار این باتری ها واکنش بین سرب و اسید سولفوریک می باشد. همچنین از اسید سولفوریک در ترکیب باتری های قوی تجهیزات تصویر برداری بیمارستانی و باتری ماشین آلات و تجهیزات کشاورزی نیز استفاده می شود.

- کاربرد اسید سولفوریک در سنتزهای شیمیایی:
اسید سولفوریک در فرآیند تولید مواد شیمیایی مانند سولفات آلومینیوم، اسید سیتریک، سولفات مس، سولفات نیکل، اسید بوریک، ایزوپروپیل الکل، اتانول از اولفین ها و دی اکسید تیتانیوم، سولفات منگنز و بلور تری گلایسین سولفات (TGS) استفاده می شود.
- کاربرد اسید سولفوریک در صنایع آبکاری:
برای پاکسازی و حل کردن آلودگی های معدنی و از بین بردن اکسید بر روی فلزات و چربی ها، قبل از آبکاری از اسید سولفوریک استفاده می کنند. اما برای آبکاری برنج بر روی سرب، سولفوریک اسید، اسید خوبی نیست.

- کاربرد اسید سولفوریک در محلول های اسیدی تصفیه آب RO:
آب ورودی به دستگاه آب شیرین کن RO دارای PH خنثی و یا مقداری اسیدی است زیرا سبب افزایش حلالیت یون های فلزی در سطح ممبرین ها و در نتیجه کاهش میزان گرفتگی ممبرین ها می شود. در این جا یک واحد تزریق اسید داریم تا PH را تنظیم کند. تزریق اسید باعث کاهش PH آب می شود و از آن برای شست و شو ممبرین ها دستگاه تصفیه آب RO یا CIP استفاده می کنیم.

- کاربرد اسید سولفوریک در تولید الیاف مصنوعی:
از موارد پرکاربرد الیاف مصنوعی در صنعت نساجی، الیاف پلی آمید، پلی استر و اکرلیک است که در ساخت آن ها از اسید سولفوریک استفاده می کنیم. هنگامی که الیاف سلولز در محلول تترا آمین مس حل شوند، مایع آبی رنگی تولید می شود. هنگامی که به آن سولفوریک اسید اضافه کنیم، الیاف ابریشم مصنوعی یا ریون تولید می شود.
کالاهای نساجی بعد از این که از سالن بافندگی خارج می شوند نیاز به رفع ناخالصی ، بازبینی و ترمیم احتمالی دارند. از اسید سولفوریک برای از بین بردن ناخالصی و رنگدانه های اضافی استفاده می شود.

- کاربرد اسید سولفوریک در صنعت چرم سازی:
اسید سولفوریک به دلیل قدرت هیدرولیز بسیار قوی، قادر به حل نمودن چربی ها و لیپیدها می باشد و به دلیل همین خاصیت در صنعت چرم سازی مورد استفاده قرار می گیرد زیرا می تواند چربی ها، مو و لایه های آلوده را از سطح چرم پاک کند.

بطور کلی اسید سولفوریک در صنعت چرم سازی در موارد زیر مورد استفاده قرار می گیرد:
- مو زدایی و آهک زنی چرم توسط اسید سولفوریک
- حذف سایر زوائد چرم با اسید سولفوریک
- حذف آهک از چرم به کمک اسید سولفوریک
- کاربرد اسید سولفوریک در مهمات سازی و مواد منفجره
از اسید سولفوریک در تولید مواد منفجره مانند نیتروگلیسیرین، TNT، RDX و PETN استفاده می شود. نیتروگلیسیرین ماده ای سمی است که اثرات تخریبی زیادی دارد؛ برای تولید نیتروگلیسیرین از اسیدهایی مانند اسید نیتریک و اسید سولفوریک استفاده می شود.
- کاربرد اسید سولفوریک در صنایع فولاد و متالورژی
سولفوریک اسید کاربردهای زیادی در صنایع فولاد و متالورژی دارد. این ماده در استخراج فلزاتی همچون مس، اورانیوم و وانادیوم کاربرد دارد. از اسید سولفوریک همچنین در شست و شو و آماده سازی فلزات برای رنگ زدن آن ها و پوشاندن با پوشش ضد زنگ استفاده می شود. با استفاده از این ماده ابتدا سطح فلزاتی که قرار است رنگ بخورند تمیز شده و ناخالصی ها و زنگ زدگی ها از سطح فلز زدوده میشود و سپس برای فرآیند رنگ زدن آماده می شود.

- کاربرد سولفوریک اسید در تولید داروهای شیمی درمانی
سرطان یک بیماری بسیار خطرناک است و داروهای آن نقش مهمی برای بیماران سرطانی دارند. سولفوریک اسید در ساخت و تولید داروهای شیمی درمانی که برای درمان سرطان استفاده می شود نقش به سزایی دارند.

اسید سولفوریک جزء مواد شیمیایی پرکاربرد میباشد و از دیگر کاربردهای اسید سولفوریک می توان به موارد زیر اشاره کرد:
- به عنوان یک ماده خشک کننده قوی کاربرد دارد.
- اکسید کنندگی بالا
- رنگ نقاشی (نایلون های رنگی و جوهر تحریر)
- استخراج فلزات
- تولید انواع حشره کش ها
- صنایع کاغذ سازی، تولید دستمال کاغذی، روزنامه و مقوا
- فرایندهای نیتروژن دار کردن
- کشش کاری (شکل دهی فلزات)
- صنایع تولید مواد شیمیایی
- تولید دترجنت ها
- تصفیه و پالایش روغن
- تصفیه فاضلاب های صنعتی
- فرآوری مواد معدنی
- در تولید اسید هیدروفلوریک
- تولید فنل
- تولید پروپانول
- ساخت چسب
- تولید ضد یخ
- ساخت و تولید فیلم های عکاسی
- تولید روان کننده ها
- صنعت لاستیک سازی به منظور کنترل pH
- برای تولید مواد چربی زدا و لوله بازکن
- در صنعت فولاد و آهن به منظور رسوب زدایی و بازیافت آمونیاک
- به منظور تولید سلفون و منسوجات استات
- فلزات آهنی و باتری ها
(MSDS) چه نکاتی را باید در زمان استفاده از اسید سولفوریک رعایت کرد؟

- این اسید بسیار قوی و خورنده است و در هنگام استفاده از آن باید تمامی نکات ایمنی را رعایت کنید. تماس اسید سولفوریک با بدن می تواند باعث تحریکات شدید پوستی و سوختگی و آسیب به چشم ها شود که علاوه بر ضایعات چشمی، منجر به نابینایی هم می شود. استنشاق اسید سولفوریک هم عوارضی مانند بروز سرفه و تنگی نفس و تحریک ریه ها دارد.
- اسید سولفوریک یکی از انواع اسید بوده و ماده ای بسیار خطرناک است که به شدت میل ترکیبی با آب دارد واکنش آن با آب به شدت گرماده است.
- به منظور رقیق سازی اسید سولفوریک، هرگز به آن آب اضافه نکنید، زیرا به سرعت با آب واکنش داده و باعث پاشش و جوشش اسید می گردد. نحوه ی صحیح رقیق سازی این است که اسید کم کم به آب اضافه شود.
بسته بندی اسید سولفوریک

این محصول در بسته بندی های زیر عرضه می گردد:
- گالن های 25 لیتری
- تانکر های 25 تنی
انبارداری، ذخیره سازی و حمل و نقل اسید سولفوریک
جهت انبار و ذخیره سازی اسید سولفوریک معمولا از مخازن پلاستیکی دو لایه تحت شرایط خاص استفاده می شود. جنس این مخازن و بست ها و اتصالات، از پلی اتیلن و یا پلی ونیل کلراید (PVC) است که از موادی از جنس پلی پروپیلن دین مونومر است و جهت آب بندی می توان از آن ها استفاده کرد.

آمار نشان می دهد با وجود این که کشور ما به عنوان یکی از تولیدکنندگان اسید سولفوریک با کیفیت در جهان مطرح است و حتی قیمت اسید سولفوریک تولیدی در ایران،در مقایسه با سایر کشورها رقابتی می باشد، اما باز هم کمتر از 7 درصد از این محصول به خارج از ایران صادر می شود. دلیل عمده این امر شرایط سخت جابجایی آن است.

برخی از مشتریان ما
مشتریان فامکو
 |
| گروه صنعتی قشونی |
با عرض پوزش کلیه قیمت ها در حال بروزرسانی می باشد، لطفا جهت استعلام قیمت خرید با واحد فروش تماس حاصل نمایید.
شرایط سخت حمل و نقل اسید سولفوریک سبب شده که همواره قیمت سوخت بر روی قیمت اسید سولفوریک تأثیرگذار باشد و از طرفی قیمت اسید سولفوریک همیشه متناسب با قیمت جهانی گوگرد بوده است. همچنین با توجه به مصرف بالای آن در جهان، قیمت این محصول هم از مکانیزم عرضه و تقاضا مستثنی نیست. پس در یک جمع بندی نوسانات قیمت اسید سولفوریک متاثر از سه عامل قیمت جهانی سوخت، قیمت جهانی گوگرد و بازار مصرف (عرضه و تقاضا) است.
عامل دیگری که در قیمت نهایی اسید سولفوریک موثر می باشد، نوع بسته بندی آن است. قیمت اسید سولفوریک بسته به خلوص آن تفاوت خواهد کرد.
در مجموع فروش اسید سولفوریک 98 درصد به دلیل پایداری بیشتری که دارد بالاتر است.
قیمت اسید سولفوریک
| ردیف |
شرح |
قیمت به تومان (هر کیلوگرم) |
| 1 |
قیمت اسید سولفوریک 98 درصد |
تماس بگیرید |
| 2 |
قیمت اسید سولفوریک 50 درصد |
تماس بگیرید |
| 3 |
قیمت اسید سولفوریک 35 درصد |
تماس بگیرید |































دیـــدگاهها
شما هم درباره این کالا دیدگاه ثبت کنید.
امتیاز: